



印度CDSCO---医疗器械注册
印度的医疗器械注册由卫生与家庭福利部卫生服务总局下属的中央药品标准控制组织(CDSCO) 监督。CDSCO 是印度的国家监管局 (NRA)。

医疗器械定义
自 2020 年 4 月 1 日起,医疗器械的状态扩大到之前通报的 23 种医疗器械,要求所有医疗器械根据 1940 年的《药品和化妆品法》进行注册。从 2022 年 10 月 1 日开始,所有 A 类和 B 类医疗器械必须在进口前拥有进口许可证。到 2023 年 10 月 1 日,所有剩余的尚未通知的 C 类和 D 类设备都需要获得进口许可证。目前不需要进口许可证的医疗设备仍必须在几天内通过电子门户注册其产品。
产品分类
医疗器械分为4类;A、B、C 和 D 基于风险级别。申请处理的 CDSCO 费用取决于设备分类。无论设备分类如何,申请过程都需要 6 到 9 个月。无法识别谓词设备的产品申请将被视为“创新”,可能需要额外的时间。
一旦获得批准,就会为每个列出批准产品的制造场所颁发进口许可证(又名 MD 表格 15)
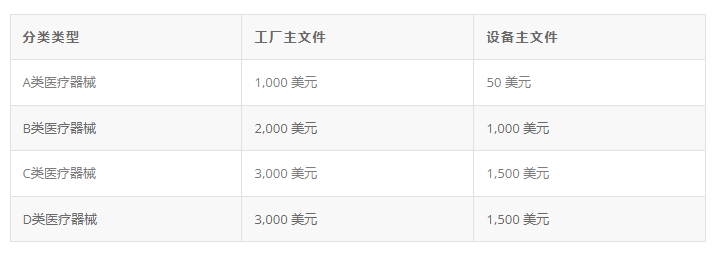
医疗器械监管途径
所有医疗器械都必须注册或拥有进口许可证,需要进口许可证的产品类型的完整列表可在本页底部找到。这些“通知”设备类别必须通过提交每个产品的设备主文件 (DMF) 和每个制造场所的工厂主文件 (PMF) 来获得进口许可证。一旦获得批准,医疗器械将根据与主要制造地点相关的进口许可证进行注册。
所有A 类和 B 类医疗器械必须在 2022 年 10 月 1 日之前获得进口许可证,以保持市场准入。其余未通知的 C 类和 D 类设备将在 2023 年 10 月 1 日之前获得进口许可证,同时需要注册为非监管产品。
进口许可证 - 设备主文件 (DMF)
印度进口器械的注册过程在很大程度上是对其现有批准的重新评估,使用参考国家所需的相同文件和证据。话虽如此,CDSCO 将非常关注应用程序的谓词设备比较部分。对于制造商来说,仔细选择比较的谓词并为等效性提供足够的证据是很重要的。
在注册期间注册的设备受益于包含管理文件的截断申请,例如来自原产国的免费销售证书、ISO 13485 证书以及基本产品信息。自愿注册过程不收取政府处理费用,但 CDSCO 可能出于产品安全考虑取消或暂停,或被强制进口许可证的要求所取代。
质量体系合格评定 - 工厂主文件 (PMF)
需要 ISO 13485 认证来证明合法和/或实际制造设施的质量体系。为了证明符合性,制造商需要为每个制造地点提交一份工厂主文件 (PMF)。一旦获得批准,将颁发进口许可证,并根据许可证添加在该地点批准的医疗器械。因此,拥有 1 个生产场地的制造商将拥有 1 个进口许可证,而拥有 3 个场地的制造商将拥有 3 个进口许可证。在 2 个地点生产的产品将需要 2 个 PMF 申请,然后在获得批准后列在每个进口许可证上。
注册创新或新型医疗器械
在材料、作用方式或预期用途方面对印度市场具有新颖性的医疗器械被视为“研究器械”,需要接受额外的临床调查要求和审查,包括通过在印度的临床调查确定安全性和有效性。这些附加要求将在与 CDSCO 召开的称为主题专家委员会 (SEC) 的会议上确定,他们将在该会议上提出附加问题,并为制造商和许可证持有人制定特定的附加要求,以保持市场准入。
非监管产品注册
所有未通知的医疗器械(下文未列出的 C 类和 D 类器械)必须按照新的强制性注册流程提交,并被称为“非监管医疗器械”。非监管注册过程将在同一天生成一个文件编号,进口商必须在将设备投放市场之前在医疗设备的标签上提及该文件编号。此非监管注册流程仅适用于 A 类和 B 类设备的 2022 年 10 月 1 日,以及 C 类和 D 类设备的 2023 年 10 月 1 日。
参考国家
有效期和续订
进口许可证不会过期,只要每 5 年支付一次上市费用。
印度CDSCO --- IVD 注册
印度的体外诊断产品注册由中央药品标准控制组织 (CDSCO)监督。2017 年新的医疗器械规则显着增加了需要完整技术文件以支持其注册申请的 IVD 设备的数量。以前只有关键的 IVD 设备需要注册完整的设备主文件,然后才能在印度投放市场。根据新规则,IVD 设备提供了基于风险的分类,所有测试套件必须在进口前获得表格 MD 15。
注册申请所需的元素包括:
1. 参考国家批准证明
2. 制造设施的 ISO 13485 认证
3. 根据设备主文件的规定要求提供完整的技术细节。
此外,与以下相关的 IVD 设备和测试套件需要美国国家生物研究所 (NIB) 的性能评估报告:
· 艾滋病病毒
· 乙肝病毒
· 血型试剂
· 血糖检测试剂
· 癌症
· 结核
· 疟疾
· 登革热
· 基孔肯雅热
· 梅毒
· 伤寒
· 流感
· ToRCH(弓形虫、风疹病毒、巨细胞病毒、单纯疱疹病毒)
· 衣原体
· 肺炎
· 耐甲氧西林金黄色葡萄球菌
· 肠病毒
· 先天性疾病标志物,例如唐氏综合症筛查测试
· 性传播媒介,即梅毒螺旋体。淋球菌、人乳头瘤病毒、疱疹病毒
· 其他危及生命的感染/病原体
性能评估报告必须由当地国家测试和校准实验室认证委员会 (NABL) 认可的实验室进行。
CDSCO 处理费因风险分类而异,如下表所示。处理时间预计需要 6 到 9 个月。成功的申请人将获得永久有效的进口许可证(又名 MD 表格 15),每五年缴纳一次保留费。
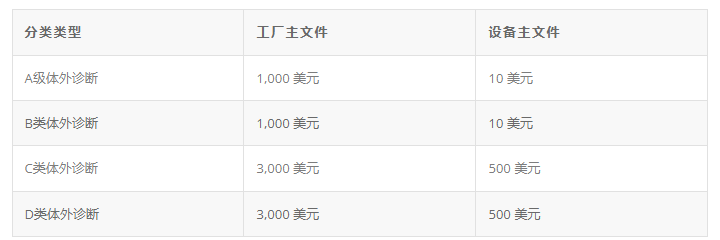
印度CDSCO---许可证持有人
许可证持有人要求
许可证持有代理被授予授权书,在当地标签上列出,处理清关和上市后的警惕。上市后警戒需要通知 CDSCO 和印度物质警戒计划 (MvPi) 印度发生的严重不良事件 (SAE)。
许可证转让
根据现行规则,不提供许可证转让,但超过 1 家公司可以持有同一产品的许可证。
使用第三方作为您的独立许可证持有者的好处
· 直接销售给多个区域分销商,避免国家进口商加价
· 提高转让定价
· 提高经销商谈判/响应中的杠杆作用
· 根据需要添加或更改分销商
· 让知识产权远离当地商业代理

-
ECE R128 欧洲车用LED灯泡E/mark标......
2024-05-08
-
2024-05-08
-
2024-05-08
-
2024-04-08
-
2024-03-14
-
2024-03-14
-
2022-09-16
-
新加坡HSA---未注册的医疗器械如何参加新加坡展......
2022-09-16
-
2022-09-07
-
2022-09-03
-
2022-01-13
-
2022-01-07


























