阿根廷ANMAT注册
阿根廷的器械分类
为您的医疗器械确定正确的分类,对于确保顺利注册过程至关重要。使用 ANMAT 发布的2318-2002 附件 II 中列出的 18 条规则确定您的设备的分类。ANMAT 分类规则与欧洲医疗器械指令 MDD 93/42/EEC 中的规则非常相似,包括修正案 2007-47-EC。
按照风险等级,分成4个类别(下图)。
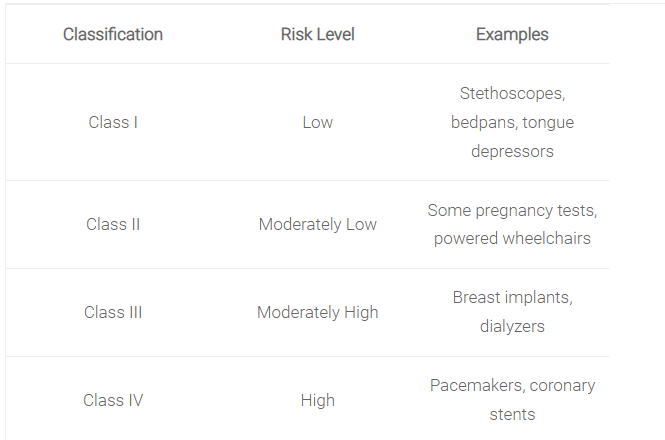
ANMAT 分类模型是基于规则的,并在南方共同市场第 40 号决议“南方共同市场医疗产品技术法规”中规定。
ANMAT 良好生产规范
阿根廷的质量体系要求与美国 FDA 21 CFR Part 820 非常相似。我们的顾问将建议您必须对现有质量体系进行哪些修改,以准备 ANMAT 质量体系认证审核。
ANMAT 需要来自公认国家的自由销售证书 - 澳大利亚、加拿大、日本、美国、欧盟。如果设备没有来自公认国家的 CFS,则需要良好生产规范 (GMP) 证书,该证书类似于 ISO 13485 和 QSR。
重要提示:所有植入物、宫内节育器和血袋都需要按照 ISO 14971 进行风险管理。
ANMAT证书有效期:5年
ANMAT注册周期:1-12个月

阿根廷授权代表 (AAR)
如果您在阿根廷没有直销办事处,那么让第三方独立公司控制您的设备的注册至关重要。ANMAT 要求寻求授权的医疗器械公司的当地代表在整个注册过程中担任联系
AAR 必须获得涵盖设备提交的 ANMAT 良好生产规范 (GMP) 认证,并持有授权许可。
出口商必须指定当地的医疗进口商或代表公司,作为注册持有人提交产品注册申请,并将作为与 ANMAT 的联系点。
进口商/代表必须经过 ANMAT 的正式注册和授权
(具有经批准的建筑基础设施、仓库和相应区域,以及技术总监等要求)。注册持有人可能不止一个。
出口商或制造商需要有原产国医疗注册证书。
需要注意的是,即使产品在另一个南方共同市场国家注册,除非在阿根廷的 ANMAT 注册,否则其注册将被视为无效。
可能需要其他文件,例如电气安全认证、制造流程图和描述;灭菌方法和参数;科学或临床证据报告。
阿根廷ANMAT注册资料要求:
· 自由销售证明 (CFS) 或外国政府证明 (CFG)
· 商业化历史
· 技术文件卷宗
· 注册费支付证明
· 南方共同市场符合性声明
· 报告召回和现场安全纠正措施的宣誓书
注意:对于 I 类设备,AAR 只需提交付款证明、制造商信息和南方共同市场符合性声明。
· 自由销售证明 (CFS)/外国政府证明: CFS 或 CFG 必须由与 ANMAT 达成协议的国家的公认权威机构提供,该协议持有有关医疗器械及其适用配件的信息以及制造商的名称.
· 技术文档的西班牙语翻译:提交给 ANMAT 的所有文件必须是西班牙语。此外,提交给 ANMAT 的档案必须具有:器械分类、使用说明 (IFU)、标签、制造商信息和技术文件。
医疗器械公司开拓阿根廷市场需要考虑的因素
对于希望拓展阿根廷多元化市场的医疗器械公司而言,有几个重要因素需要考虑:
· 南方共同市场共同对外关税 (AEC):所有进口医疗器械均需按 AEC 征税。税收范围取决于产品是否翻新(0%-24%)或不翻新(0%-16%)。
· 增值税:购买医疗器械时,需缴纳增值税。税收范围取决于产品的保险、成本和运费 (CIF) 价值。
· 审核时间和有效期:提交的标准审核时间为 180 天。但是,通常情况下,I 类医疗器械会在 30-60 天内进行审查,而所有其他器械可能需要长达一年的时间。如果产品获得批准,在阿根廷市场的有效期为5年。
· 上市后监测:医疗器械制造商必须监测和报告对其产品的任何召回,并进行上市后研究。
· 阿根廷前景比较好的医疗产品:电诊断设备,超声波设备和其他医疗设备,植入物、支架、心脏瓣膜、起搏器,专业的一次性用品